专利摘要
提供光致变色化合物,其可以是吡喃、嗪、或俘精酸酐。该光致变色化合物具有至少一个连接至其的取代基Q,各个Q独立地是-N3,-CN,-COOR′,-CCR′,-C(R′)C(R′)R′,-OCOR′,-OCOOR′,-SR′,-OS02R”’,和/或CON(R′)R′,其中各个R′是氢、取代或者非取代的具有1-8个碳原子的烷基,非取代或者取代的芳基,具有2-18个碳原子的非取代的或者取代的链烯基或者炔基,其中该取代基是卤素或者羟基以及R”’是CF3或者具有2-18个碳原子的全氟代烷基。组成部分Q的个数、位置和特性取决于该光致变色化合物的结构。
说明书
相关申请的交叉引用
本申请是2004年5月17日提交的申请号为US 10/846,629的美国专利申请的部分继续申请,在本文中明确将其引入作为参考以及进而其要求2003年7月1日提交的申请号为60/484,100的美国临时申请的权益。
有关联邦政府资助研究或者开发的声明
不适用。
有关序列表
不适用。
背景技术
本申请所公开各种非限制实施方案通常涉及光致变色化合物。其它非限制实施方案涉及使用本申请公开的光致变色化合物制造的装置与元件。
常规光致变色化合物具有至少两种状态,具有第一吸收光谱的第一状态以及具有不同于第一吸收光谱的第二吸收光谱的第二状态,以及至少对光化学辐射响应而能够在该两个状态之间转换。此外,常规光致变色化合物可以是热可逆的。也就是,常规光致变色化合物能够至少对光化学辐射响应而在第一状态与第二状态之间转换以及对热能响应而恢复到第一状态。如本文所用″光化学辐射″意指电磁辐射,比如紫外线以及能引起响应的可见光辐射。更具体地说,常规光致变色化合物能对光化学辐射响应而进行从一种异构体到另一种异构体的变换,且各异构体具有特征吸收光谱,以及还可对热能响应而恢复到第一异构体(即,是热可逆的)。例如,常规的热可逆的光致变色化合物通常能够对光化学辐射响应而从第一状态例如″透明状态,″改变至第二状态,例如″彩色状态,″以及对热能响应而恢复到″透明″状态。
二色性化合物是能够对穿透辐射中两正交平面偏振分量(orthogonal plane polarized components)之一的吸收强于另一分量的化合物。因此,二色性化合物能够使穿透辐射线偏振(polarizing)。如本文所用,″线偏振″意指将光波电场矢量振动限制至一个方向或者平面。然而,尽管二色性材料能够优先吸收穿透辐射的两正交平面偏振组分之一,但是如果二色性化合物分子不适宜地定位或者排列,则无法获得穿透辐射净线偏振。也就是,由于该二色性化合物分子无规定位,各个分子选择吸收可能互相抵消以致无法获得净或者总体线偏振作用。因此,通常需要在另外的材料之内适宜地定位或者排列该二色性化合物分子以形成常规线性偏振元件,比如线偏振过滤器或者用于太阳眼镜的透镜。
与该二色性化合物相反,通常不需要定位或者排列常规光致变色化合物分子以形成常规光致变色元件。因此,例如,常规光致变色元件、比如用于光致变色眼镜的透镜,可以通过例如在透镜的表面上旋涂包含常规光致变色化合物以及″主体″材料的溶液,以及适宜不按任何特定取向排列该光致变色化合物而固化所产生的涂层或者层而形成。此外,即使常规光致变色化合物分子适宜按以上关于该二色性化合物的讨论来定位或者排列,但因为常规光致变色化合物不强烈显示二色性,所以由此制造的元件通常线偏振不强烈。
提供可以在至少一状态中显示出有用光致变色和/或二色性性能的光致变色化合物将会是有益的而且其可被用于各种应用以给与光致变色和/或二色性性能。
附图说明
本发明各个非限制性实施方案如果结合附图解读则将更好地理解,其中:
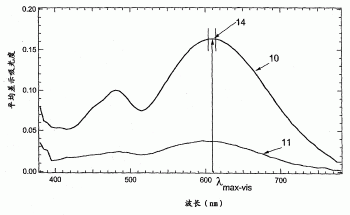
图1显示针对本申请公开的各个非限制实施方案所述光致变色化合物使用CELL法获得的两平均差吸收光谱。
图2显示根据本发明所述,制备具有不同Q基团的光致变色化合物(PC)的总反应图解。
图3以及4根据本发明所述,各自显示制备具有不同的Q基团萘酚的总反应图解。
图5显示根据本发明所述,用于制备茚并-稠合萘酚的反应图解。
图6显示制备本发明所述萘酚的反应图解。
发明详述
在说明书中和所附权利要求中所使用的冠词“a”,“an”和“the”包括复数指代物,除非特意地和明确地限于一个指代物。
另外,对于本说明书而言,除非另有说明,表达成分的量、反应条件和在说明书中使用的其它性能或参数的所有数值被理解为在一切情况下被术语“约”修饰。因此,除非另有说明,应当理解在下面的说明书和所附权利要求中给出的数值参数是近似值。至少,并且不试图将等同原则的应用限于权利要求的范围,各数值参数应该至少按照报道的有效数字的数值并采用寻常的舍入技术来读取。
此外,尽管表达本发明的宽范围的数值范围和参数设定值是如以上所讨论的近似值,但是在实施例部分中给出的数值尽可能准确地报道。然而,应该理解的是,此类数值固有地含有由测量设备和/或测量技术引起的一定误差。
现在描述本发明各个非限制性实施方案。一个非限制实施方案提供一种热可逆、光致变色化合物,其在下文所述位置具有Q基团以及任选也在下文所述的延长基团L。另外的非限制性实施方案提供光致变色化合物,其适合于具有至少第一状态以及第二状态,其中该热可逆、光致变色化合物根据CELL法测定的平均吸收比与在至少一状态中的相比高2.3,其在以下详细公开。此外,根据在各个非限制实施方案中所述的,其中该热可逆、光致变色化合物根据CELL法测定的平均吸收比与在活化态中的相比高2.3。如本文所用,该术语″光致变色化合物″(PC)包括热可逆光致变色化合物,选自茚并[2′,3′-3,4]萘并[1,2-b]吡喃、茚并[3′,2′-3,4]萘并[1,2-b]吡喃、噻吩并[2′,3′-3,4]萘并[1,2-b]吡喃、噻吩并[3′,2′-3,4]萘并[1,2-b]吡喃、苯并噻吩并[2′,3′-3,4]萘并[1,2-b]吡喃、苯并噻吩并[3′,2′-3,4]萘并[1,2-b]吡喃、呋喃并[2′,3′-3,4]萘并[1,2-b]吡喃、呋喃并[3′,2′-3,4]萘并[1,2-b]吡喃、苯并呋喃并[2′,3′-3,4]萘并[1,2-b]吡喃、苯并呋喃并[3′,2′-3,4]萘并[1,2-b]吡喃、2H-萘并[1,2-b]吡喃、3H-萘并[2,1-b]吡喃、苯并吡喃、螺[1,3-二氢吲哚-3,3′-萘并[2,1-b][1,4]] 嗪、螺[1,3-二氢吲哚-2,2′-萘并[1,2-b][1,4]] 嗪和俘精酸酐及其混合物。如本文所用的就光致变色化合物而言的该术语″活化态″,指该光致变色化合物当暴露于足够光化学辐射以致使该光致变色化合物至少一部分转换状态。此外,如本文所用术语″化合物″,意指物质由两种或更多种元素、组分、成分、或者组成部分以及无限制包括由两种或更多种元素、组分、成分、或者组成部分形成的分子以及高分子(例如聚合物或者低聚物)联合形成。
一般而言,测量光致变色化合物的平均吸收比的CELL法包括在两个正交偏振方向的每一个方向上获得光致变色化合物在活化状态或未活化状态下的吸收光谱,同时光致变色化合物在包含于CELL组装体内的定向液晶介质中至少部分地定向。更具体地说,该CELL组装体包括以20微米+/-1微米的间距间隔的两个相对的玻璃基板。基板沿着两个相对的边缘密封,形成CELL。每一玻璃基板的内表面涂敷了聚酰亚胺涂层,涂层的表面通过摩擦至少部分地有序化。光致变色化合物的定向可以通过将光致变色化合物和液晶介质引入到CELL组装体中和使液晶介质沿摩擦的聚酰亚胺表面定向来实现。因为光致变色化合物包含在液晶介质内,液晶介质的定向致使光致变色化合物被定向。本领域中的那些技术人员会认识到,液晶介质的选择和在试验过程中使用的温度会影响所测量的吸收比。因此,如在实施例中更详细地阐明,对于CELL法,吸收比测量是在室温(73℉+/-0.5℉或更好)下进行,液晶介质是Licristal E7(它被报道是氰基联苯基和氰基三联苯基液晶化合物的混合物)。
一旦液晶介质和光致变色化合物已定向,将CELL组装体(cell assembly)放置于光具座(在实施例中更详细地描述它)上。为了获得在活化状态下的平均吸收比,通过将光致变色化合物暴露于紫外线辐射中一段时间来实现光致变色化合物的活化,该时间足以达到饱和或接近饱和状态(即,其中在测量过程中经过一定时间间隔之后光致变色化合物的吸收性能基本上不改变的一种状态)。对于在与光具座垂直的平面(称作0°偏振平面或方向)上线性偏振的光以及在与光具座平行的平面(称作90°偏振平面或方向)上线性偏振的光以3秒间隔经过一段时间(典型地10-300秒),按照下列顺序:0°,90°,90°,0°等来进行吸收测量。线性偏振光被CELL吸收的吸收率是针对全部所试验波长在每一时间间隔中测量的,在相同波长范围中的未活化吸收率(即具有液晶材料和未活化的光致变色化合物的池的吸收率)被扣除而在0°和90°偏振平面的每一个平面中获得光致变色化合物的吸收光谱,从而获得处于饱和或接近饱和状态下的光致变色化合物在各偏振平面上的平均差异吸收光谱。
例如,参考图1,显示了对于根据本申请公开的一个非限制性实施方案的光致变色化合物所获得的在一个偏振平面上的平均差异吸收光谱(一般表示为10)。平均吸收光谱(一般表示为11)是对于相同的光致变色化合物在正交偏振平面上所获得的平均差异吸收光谱。
以对于光致变色化合物所获得的平均差异吸收光谱为基础,如下获得了光致变色化合物的平均吸收比。根据下列等式计算在与λmax-vis+/-5纳米(在图1中一般表示为14)对应的预定波长范围内的每一波长下光致变色化合物的吸收比,其中λmax-vis是光致变色化合物在任何平面上具有最高平均吸收率的那一波长:
ARλi=Ab1λi/Ab2λi 等式1
其中,ARλi是在波长λi下的吸收比,Ab1λi是在具有较高吸收率的偏振方向(即,0°或90°)上在波长λi下的平均吸收率,和Ab2λi是在剩余偏振方向上在波长λi下的平均吸收率。如前面所讨论,“吸收比”指在第一平面上线性偏振的辐射的吸收率与在与第一平面正交的平面上线性偏振的相同波长辐射的吸收率的比率,其中第一平面取作具有最高吸收率的平面。
然后根据下列方程式,通过将对于在预定波长范围(即,λmax-vis+/-5纳米)内的波长所获得的各吸收比平均化来计算光致变色化合物的平均吸收比(“AR”):
AR=(∑ARλi)/ni 等式2
其中,AR是光致变色化合物的平均吸收比,ARλi是在预定波长范围(即,λmax-vis+/-5纳米)内的各波长的各自吸收比(按照以上在等式1中测定),和ni是平均化的各吸收比的数目。
如前面所讨论,普通的热可逆光致变色化合物适合于对光化辐射作出响应从第一状态转换到第二状态,并对热能作出响应恢复到第一状态。更具体地说,普通的热可逆、光致变色的化合物能够响应于光化辐射从一种异构体形式(例如和没有限制地,闭合形式(closed form))转换到另一种异构体形式(例如和没有限制地,开口形式(open form)),和当暴露于热能时恢复到闭合形式。然而,如前面所讨论,一般来说普通的热可逆的光致变色化合物没有强烈地显示二色性。
如以上所讨论,本申请公开的非限制性实施方案提供了具有根据CELL法测定的在至少一种状态下大于2.3的平均吸收比的热可逆光致变色化合物和/或可以用作制备吸收比大于2.3的光致变色化合物的中间体的热可逆光致变色化合物。因此,根据此非限制性实施方案所述的热可逆光致变色化合物能够显示出有用的光致变色性能和/或有用的光致变色性能和二色性性能。即,该热可逆、光致变色的化合物可以是热可逆、光致变色和/或光致变色-二色性化合物。就本申请所公开的光致变色化合物而言,本申请所使用的术语“光致变色-二色性”指在某些条件下同时显示出光致变色和二色性性能,这些性能至少可以由仪器检测到。
根据其它非限制性实施方案所述,热可逆的光致变色化合物可以是在至少一种状态下具有根据CELL法测定的从4到20,从3到30,或从2.5到50的平均吸收比的热可逆光致变色-二色性化合物。本领域技术人员会认识到,光致变色化合物的平均吸收比越高,光致变色化合物更加线性地偏振。因此,根据各种非限制性实施方案,热可逆光致变色化合物能够具有为了达到所要求程度的线性极化所需的任何平均吸收比。
另一个非限制性实施方案提供热可逆的、光致变色的化合物,它不含 嗪并适于具有至少第一状态和第二状态,其中光致变色化合物在至少一种状态下具有根据CELL法测定的至少1.5的平均吸收比。此外,根据这一非限制性实施方案,平均吸收比能够在至少一种状态下是根据CELL法测定的1.5-50。
在本发明的具体实施方案中,提供光致变色材料,其包含茚并[2′,3′-3,4]萘并[1,2-b]吡喃、茚并[3′,2′-3,4]萘并[1,2-b]吡喃、噻吩并[2′,3′-3,4]萘并[1,2-b]吡喃、噻吩并[3′,2′-3,4]萘并[1,2-b]吡喃、苯并噻吩并[2′,3′-3,4]萘并[1,2-b]吡喃、苯并噻吩并[3′,2′-3,4]萘并[1,2-b]吡喃、呋喃并[2′,3′-3,4]萘并[1,2-b]吡喃、呋喃并[3′,2′-3,4]萘并[1,2-b]吡喃、苯并呋喃并[2′,3′-3,4]萘并[1,2-b]吡喃、苯并呋喃并[3′,2′-3,4]萘并[1,2-b]吡喃、2H-萘并[1,2-b]吡喃、3H-萘并[2,1-b]吡喃、苯并吡喃、螺[1,3-二氢吲哚-3,3′-萘并[2,1-b][1,4]] 嗪、螺[1,3-二氢吲哚-2,2′-萘并[1,2-b][1,4]] 嗪或者俘精酸酐;其中:
(A)所述光致变色材料具有至少一个取代基Q,其连接至在下文指定的特定碳原子,各Q独立地包含-N3、-CN、-COOR′、-CCR′、-C(R′)C(R′)R′、-OCOR′、-OCOOR′、-SR′、-OSO2R″′、和/或-CON(R′)R′,其中各R′独立地包含氢、未被取代的或者取代的1-18个碳原子烷基、未被取代的或者取代的芳基、未被取代的或者取代的2-18个碳原子的烯基或者炔基,其中所述取代基选自卤素以及羟基以及R″′包含-CF3或者具有2-18个碳原子的全氟代烷基;条件是其中:
(a)当所述光致变色材料包含茚并[2′,3′-3,4]萘并[1,2-b]吡喃、茚并[3′,2′-3,4]萘并[1,2-b]吡喃、噻吩并[3′,2′-3,4]萘并[1,2-b]吡喃、噻吩并[3′,2′-3,4]萘并[1,2-b]吡喃、苯并噻吩并[2′,3′-3,4]萘并[1,2-b]吡喃、苯并噻吩并[3′,2′-3,4]萘并[1,2-b]吡喃、呋喃并[2′,3′-3,4]萘并[1,2-b]吡喃、呋喃并[3′,2′-3,4]萘并[1,2-b]吡喃、苯并呋喃并[2′,3′-3,4]萘并[1,2-b]吡喃、苯并呋喃并[3′,2′-3,4]萘并[1,2-b]吡喃,Q连接至7-和/或10-位以及包含-N3、-COOR′、-CCR′、-C(R′)C(R′)R′、-OCOR′、-OCOOR′、-SR′、-OSO2R″′或者-CN,条件是当所述光致变色材料是茚并[2′,3′-3,4]萘并[1,2-b]吡喃时,所述材料化合物在12-位基本上不含取代基;
(b)当所述光致变色材料包含3H-萘并[2,1--b]吡喃时,Q连接至其6-和/或7-位以及对于各个情况独立地包含-N3或者-OCOOR′;
(c)当所述光致变色材料包含2H-萘并[1,2-b]吡喃,Q连接至其8-位以及包含-N3;或者-OCOOR′,条件是所述光致变色材料在5-位基本上无取代基;
(d)当所述光致变色材料包含苯并吡喃时,Q连接至其7-位以及包含-N3、-CN、-CCR′、或者-OSO2R″′;
(e)当所述光致变色材料包含螺[1,3-二氢吲哚-2,2′-萘并[1,2-b][1,4]] 嗪,取代基Q连接至其5-、6-和/或8′-位以及对于各个情况独立地包含-N3;-CCR′,条件是该″′吲哚并(indolino)基团基本上不含N-取代基;或者-OSO2R″′,条件是所述光致变色材料基本上不含羰基;
(f)当所述光致变色材料包含螺[1,3-二氢吲哚-2,3′-萘并[2,1-b][1,4]] 嗪时,取代基Q连接至其5-、6-、6′和/或7′-位以及对于各个情况独立地包含-N3;-CCR′,条件是吲哚并基团基本上不含N-取代基;或者-OSO2R″′,条件是所述光致变色材料基本上不含羰基;以及
(g)当所述光致变色材料包含俘精酸酐时,Q包含-N3,-CN,-CCR′,或者-OSO2R″′;以及
(B)任选,所述光致变色材料具有至少一种延长剂L,由以下式表示(其在以下详细公开):
-[S1]c-[Q1-[S2]d]d′-[Q2-[S3]e]e′-[Q3-[S4]f]f′-S5-P
在这里使用的术语“连接”指直接键接或经由另一个基团间接地键接。因此,例如,根据本申请公开的各种非限制性实施方案,L能够作为在PC上的取代基直接键接于PC上,或L能够是在直接键接于PC上的另一个基团(如由R表示的基团,它在下面将讨论)上的取代基(即,L间接地键接到PC上)。虽然在本申请并非限制,根据各种非限制性实施方案,L能够连接于PC上,从而在活化状态下使PC延伸或延长,这样所延伸PC(即,光致变色化合物)的吸收比与单独PC相比得到了增强。虽然在本申请并非限制,根据各种非限制性实施方案,L在PC上的连接位置能够进行选择,以使得在与活化形式PC的理论过渡偶极矩平行或垂直的方向中至少一个方向上L使PC延长。就L位置而言,其可以随后在Q基团处连接至光致变色化合物。本申请光致变色化合物在指明位置可以具有至少一个Q基团以及任选一个或多个L基团。本申请使用的术语“理论过渡偶极矩”指通过电磁辐射与分子的相互作用所产生的瞬时偶极极化。参见,例如,IUPAC Compendium of Chemical Technology,第二版,国际纯粹与应用化学联合会(1997)。
就以上L而言,各Q1、Q2和Q3能够在各情况下独立地选自:从未被取代的或取代的芳基、未被取代的或取代的脂环族基、未被取代的或取代的杂环基团以及它们的混合基团中选择的二价基团,其中取代基选自:由P表示的基团,液晶基团(mesogen),卤素,多(C1-C18烷氧基),C1-C18烷氧基羰基,C1-C18烷基羰基,C1-C18烷氧基羰基氧基,芳氧基羰基氧基,全氟(C1-C18)烷氧基,全氟(C1-C18)烷氧基羰基,全氟(C1-C18)烷基羰基、全氟(C1-C18)烷基氨基,二(全氟(C1-C18)烷基)氨基,全氟(C1-C18)烷基硫基,C1-C18烷基硫基,C1-C18酰基,C3-C10环烷基,C3-C10环烷氧基,被氰基、卤素或C1-C18烷氧基单取代或被卤素多取代的直链或支化C1-C18烷基,和由下列通式中的一种表示的基团:-M(T)(t-1)和-M(OT)(t-1),其中M选自铝,锑,钽,钛,锆和硅,T选自有机官能化基团,有机官能化烃基,脂族烃基和芳族烃基,以及t是M的价态。在这里使用的前缀“多”指至少两个。
如以上所讨论,Q1,Q2和Q3能够独立地在各情况下选自二价基团,如未被取代的或取代的芳基,未被取代的或取代的杂环基团,和未被取代的或取代的脂环族基。有用的芳族基的非限制性例子包括:苯并,萘并,菲并,联苯基,四氢萘并,三联苯基,和蒽并。
在这里使用的术语“杂环基团”指具有原子的环的化合物,其中构成环的至少一个原子不同于构成环的其它原子。此外,本申请使用的术语“杂环基团”具体地说排除稠合杂环基团。从中可以选择出Q1、Q2和Q3的合适杂环基团的非限制性例子包括:异山梨醇(isosorbitol),二苯并呋喃并,二苯并噻吩并,苯并呋喃并,苯并噻吩并,噻吩并,呋喃并,二氧己并(dioxino),咔唑并,氨茴内酐基(anthranilyl),吖庚因基(azepinyl),苯并 唑基,二吖庚因基(diazepinyl),二唑基(dioazlyl),咪唑烷基,咪唑基,咪唑啉基,吲唑基,假吲哚基(indoleninyl),二氢吲哚基(indolinyl),中氮茚基,吲哚基,吲哚 嗪基,异吲哚基,异氮杂茚基,异 唑基(isooxazolyl),isooxazyl,异吡咯基,异喹啉基,异噻唑基,吗啉代,吗啉基, 二氮杂唑基(oxadiazolyl),噻唑基, 噻唑基(oxathiazolyl),氧硫杂环戊二烯(oxathiolyl), 三唑基(oxatriazolyl), 唑基,哌嗪基,piperazyl,哌啶基,嘌呤基,吡喃并吡咯基,吡嗪基,吡唑烷基,吡唑啉基,吡唑基,pyrazyl,哒嗪基,pyridazyl,吡啶基,嘧啶基(pyrimidinyl),pyrimidyl,,pyridenyl,吡咯烷基,吡咯啉基,吡咯甲酰基(pyrroyl),喹嗪基(quinolizinyl),奎宁环基,喹啉基,噻唑基,三唑基,triazyl,N-芳基哌嗪基,氮丙啶并,芳基哌啶子基,硫代吗啉代,四氢喹啉并,四氢异喹啉并,吡咯基,未被取代的、单-或二-取代的C4-C18螺双环胺,以及未被取代的、单-或二-取代的C4-C18螺三环胺。
如以上所讨论,根据各种非限定性实施方案,Q1,Q2和Q3能够选自单-或二-取代的C4-C18螺双环胺和C4-C18螺三环胺。合适取代基的非限制性例子包括芳基,C1-C6烷基,C1-C6烷氧基或苯基(C1-C6)烷基。单-或二-取代的螺双环胺的特定的非限制性例子包括:2-氮杂双环[2.2.1]庚-2-基;3-氮杂双环[3.2.1]辛-3-基;2-氮杂双环[2.2.2]辛-2-基;和6-氮杂双环[3.2.2]壬-6-基。单-或二取代的三环胺的特定的非限制性例子包括:2-氮杂三环[3.3.1.1(3,7)]癸-2-基;4-苄基-2-氮杂三环[3.3.1.1(3,7)]癸-2-基;4-甲氧基-6-甲基-2-氮杂三环[3.3.1.1(3,7)]癸-2-基;4-氮杂三环[4.3.1.1(3,8)]十一烷-4-基;和7-甲基-4-氮杂三环[4.3.1.1(3,8)]十一烷-4-基。
从中可以选择出Q1,Q2,和Q3的脂环族基的例子包括,而不限于,环己基,环丙基,降冰片烯基,十氢萘基,金刚烷基,双环辛烷,全氢芴,和立方烷基。
继续关于L,各S1,S2,S3,S4和S5在各情况下独立地选自下列这些的间隔单元:
(1)-(CH2)g-,-(CF2)h-,-Si(CH2)g-,-(Si[(CH3)2]O)h-,
其中g在各情况下独立地选自1到20;h选自1到16,包括端值;
(2)-N(Z)-,-C(Z)=C(Z)-,-C(Z)=N-,-C(Z′)-C(Z′)-,或者单键,其中Z在各情况下独立地选自氢,C1-C6烷基,C3-C10环烷基和芳基,和Z′在各情况下独立地选自C1-C18烷基,C3-C10环烷基和芳基;和
(3)-O-,-C(O)-,-C≡C-,-N=N-,-S-,-S(O)-,-S(O)(O)-,-(O)S(O)O-,-O(O)S(O)O-直链或支化C1-C24亚烷基残基,所述C1-C24亚烷基残基是未被取代的,被氰基或卤素单取代,或被卤素多取代;条件是当两个包括杂原子的间隔单元联接在一起时,该间隔单元在联接时要求杂原子不直接联接于彼此之上以及当S1和S5分别地联接到PC和P上时,它们在联接时要求两个杂原子不直接联接于彼此之上。在这里使用的术语“杂原子”指除碳或氢之外的原子。
根据在这里公开的各种非限制性实施方案,在L中,c,d,e和f可以各自独立地选自1-20中的整数,包括端值;和d′,e′和f′可以各自独立地选自0,1,2,3和4,前提条件是d′+e′+f′的总和至少是1。根据本申请公开的其它非限制性实施方案,c,d,e和f可以各自独立地选自0-20中的整数,包括端值;和d′,e′和f′可以各自独立地选自0,1,2,3和4,前提条件是d′+e′+f′的总和至少是2。根据在这里公开的另一非限制性实施方案,c,d,e和f可以各自独立地选自0-20中的整数,包括端值;和d′,e′和f′可以各自独立地选自0,1,2,3和4,前提条件是d′+e′+f′的总和至少是3。根据在本申请公开的又一非限制性实施方案,c,d,e和f可以各自独立地选自0-20中的整数,包括端值;和d′,e′和f′可以各自独立地选自0,1,2,3和4,前提条件是d′+e′+f′的总和至少是1。
此外,在L中,P可以选自:羟基、氨基、C2-C18烯基、C2-C18炔基、叠氮基、甲硅烷基、甲硅烷氧基、甲硅烷基氢化物、(四氢-2H-吡喃-2-基)氧基、硫醇基、异氰酸根合、硫代异氰酸根合、丙烯酰氧基、甲基丙烯酰氧基、2-(丙烯酰氧基)乙基氨基甲酰基、2-(甲基丙烯酰氧基)乙基氨基甲酰基、氮丙啶基、烯丙氧基羰氧基、环氧基、羧酸基、羧酸酯基、丙烯酰基氨基、甲基丙烯酰基氨基、氨羰基、C1-C18烷基氨羰基、氨羰基(C1-C18)烷基、C1-C18烷氧基羰基氧基、卤代羰基、氢、芳基、羟基(C1-C18)烷基、C1-C18烷基、C1-C18烷氧基、氨基(C1-C18)烷基、C1-C18烷基氨基、二-(C1-C18)烷基氨基C1-C18烷基(C1-C18)烷氧基、C1-C18烷氧基(C1-C18)烷氧基、硝基、聚(C1-C18)烷基醚、(C1-C18)烷基(C1-C18)烷氧基(C1-C18)烷基、聚氧化乙烯、聚氧化丙烯、乙炔基(ethylenyl)、丙烯酰基、丙烯酰氧基(C1-C18)烷基、甲基丙烯酰基、甲基丙烯酰氧基(C1-C18)烷基、2-氯代丙烯酰基、2-苯基丙烯酰基、丙烯酰氧基苯基、2-氯代丙烯酰基氨基、2-苯基丙烯酰基氨基羰基、oxetanyl、缩水甘油基、氰基、异氰酸根合(C1-C18)烷基、衣康酸酯、乙烯基醚、乙烯基酯、苯乙烯衍生物、主链和侧链液晶聚合物、硅氧烷衍生物、乙撑亚胺衍生物、马来酸衍生物、富马酸衍生物、未取代肉桂酸衍生物、肉桂酸衍生物用至少甲基、甲氧基、氰基以及卤素之一取代的物质、或者取代或者未被取代的手性的或者非手性的单价的或者二价基团,其选自类固醇基团、萜类化合物基团、生物碱基团及其混合物,其中该取代基独立地选自C1-C18烷基、C1-C18烷氧基、氨基、C3-C10环烷基、C1-C18烷基(C1-C18)烷氧基、氟代(C1-C18)烷基、氰基、氰基(C1-C18)烷基、氰基(C1-C18)烷氧基或其混合物,或者P是一种结构,其具有2-4个反应性基团或者P是未被取代的或者取代的开环易位聚合前体。
根据在这里公开的各种非限制性实施方案,当P是可聚合的基团时,可聚合的基团能够是适于参与到聚合反应中的任何官能团。聚合反应的非限制性例子包括描述在Hawley′s Condensed Chemical Dictionary Thirteenth Edition,1997中的“polymerization”的定义中的那些,John Wiley&Sons,第901-902页,它的公开内容被引入这里供参考。例如,虽然在这里没有限制,聚合反应包括:“加成聚合”,其中自由基是引发剂,它通过在单体双键的一侧上加成到单体上和同时在另一侧上产生新的自由电子来与单体双键反应;“缩聚”,其中两个反应用分子相结合形成更大的分子,同时消去小分子如水分子;和“氧化偶联聚合”。此外,可聚合的基团的非限制性例子包括羟基,丙烯酰氧基,甲基丙烯酰氧基,2-(丙烯酰氧基)乙基氨基甲酰基,2-(甲基丙烯酰氧基)乙基氨基甲酰基,异氰酸酯,氮杂环丙烷,烯丙基碳酸酯,和环氧基,例如,环氧乙烷基甲基。
根据一个特定的非限制性实施方案,P能够选自主链或侧链液晶聚合物和液晶基团。本申请使用的术语液晶“基团(mesogen)”指刚性棒状或圆盘状液晶分子。此外,在这里使用的术语“主链液晶聚合物”指在聚合物的骨架(即,该主链)结构中具有液晶基团的聚合物。本申请使用的术语“侧链液晶聚合物”指在侧链中具有连接于聚合物上的液晶基团的聚合物。虽然在本申请没有限制,一般,基团是由限制液晶聚合物的运动的两个或更多个芳族环构成的。合适棒状液晶基团的例子包括而不限于:取代的或未被取代的芳族酯,取代的或未被取代的线性芳族化合物,以及取代的或未被取代的三联苯类。
根据另一个特定的非限制性实施方案,P能够选自甾类基团,举例说且不限于,胆甾醇类化合物。
如以上所讨论,本申请公开的各种非限制性实施方案提供光致变色化合物,它包括(a)光致变色基团(PC)和(b)在上述位置处的至少一个Q基团以及任选地,连接至PC的至少一种延长剂(L)(以上)。
在备选的实施方案中,该光致变色化合物可以由以下图解式I,II,III,IVA,IVB,V或者VI表示:
其中:
(A)各个取代基Q独立地包含-N3,-CN,-COOR′,-CCR′,-OCOR′,-OCOOR′,-SR′,-OSO2R″′,和/或-CONHR′,其中各个R′包含氢、未被取代的或取代的具有1至18个碳原子的烷基、未被取代的或者取代的芳基、未被取代的或者取代的具有2-18个碳原子的烯基或者炔基,其中所述取代基选自卤素以及羟基,R″′包含-CF3或者具有2-18个碳原子的全氟代烷基;
(B)各个i是整数,选自0至可得到位置的总数以及各R在各个情况下独立选自:
(a)在下文公开的B表示的基团;
(b)-C(O)X24,其中X24选自延长剂L、羟基、C1-C18烷基、C1-C18烷氧基、未被取代的苯基或者用C1-C18烷基或者C1-C18烷氧基单取代的苯基、未被取代的氨基、用C1-C18烷基、苯基、苄基以及萘基中至少之一单或者二取代的氨基;
(c)-OX7以及-N(X7)2;其中X7选自:
(i)延长剂L、氢、C1-C18烷基、C1-C18酰基、苯基(C1-C18)烷基、单(C1-C18)烷基取代苯基(C1-C18)烷基、单(C1-C18)烷氧基取代苯基(C1-C18)烷基;C1-C18烷氧基(C1-C18)烷基;C3-C10环烷基;单(C1-C18)烷基取代的C3-C10环烷基、C1-C18卤代烷基、烯丙基、苯甲酰基、单取代的苯甲酰基、萘甲酰基或者单取代的萘甲酰基,其中每一个所述苯甲酰基以及萘甲酰基取代基独立地选自C1-C18烷基、以及C1-C18烷氧基;
(ii)-CH(X8)X9,其中X8选自延长剂L、氢或者C1-C18烷基;以及X9选自延长剂L,-CN,-CF3,或者-COOX10,其中X10选自延长剂L,氢或者C1-C18烷基;
(iii)-C(O)X6,其中X6选自下述中至少之一:延长剂L、氢、C1-C18烷氧基、未被取代的苯氧基、用C1-C18烷基或者C1-C18烷氧基单或者二取代的苯氧基、未被取代的芳基、用C1-C18烷基或者C1-C18烷氧基单或者二取代的芳基、未被取代的氨基、用C1-C18烷基单或者二取代的氨基、以及苯基氨基,其是未被取代的、用C1-C18烷基或者C1-C18烷氧基单或者二取代的;或者
(iv)三(C1-C18)烷基甲硅烷基、三(C1-C18)烷基甲硅烷氧基、三(C1-C18)烷氧基甲硅烷基、三(C1-C18)烷氧基甲硅烷氧基、二(C1-C18)烷基(C1-C18烷氧基)甲硅烷基、二(C1-C18)烷基(C1-C18烷氧基)甲硅烷氧基、二(C1-C18)烷氧基(C1-C18烷基)甲硅烷基或者二(C1-C18)烷氧基(C1-C18烷基)甲硅烷氧基;
(d)-SX11;其中X11选自延长剂L,氢,C1-C18烷基,C1-C18卤代烷基,芳基,其是未被取代的、或者用C1-C18烷基、C1-C18烷氧基、或者卤素单或者二取代的;
(e)式i表示的含氮的环:
其中:
(i)n是选自0,1,2和3的整数,条件是,如果n是0,则U′是U并且每个U在各情况下独立地选自-CH2-、-CH(X12)-、-C(X12)2-、-CH(X13)-、-C(X13)2-、和-C(X12)(X13)-,其中X12选自延长剂L和C1-C18烷基,X13选自延长剂L、苯基和萘基,以及
(ii)U′选自U、-O-、-S-、-S(O)-、-NH-、-N(X12)-或-N(X13)-,m是选自1、2和3的整数;
(f)由式ii或iii表示的基团;
其中X14,X15,和X16各种情况下独立选自延长剂L,氢,C1-C18烷基,苯基或萘基,或者X14和X15一起形成5-8个碳原子的环;p是整数,选自0,1,或2,X17各种情况下独立选自延长剂L,C1-C18烷基,C1-C18烷氧基,或者卤素;
(g)相紧邻基团R一起连接形成由式vii,viii,或ix表示的基团:
其中
(i)W和W′在各情况下独立地选自-O-,-N(X7)-,-C(X14)-,和-C(X17)-;
(ii)X14,X15和X17,其中X14,和X15各种情况下独立选自延长剂L,氢,C1-C18烷基,苯基或萘基,或者X14和X18一起形成5-8个碳原子的环;以及X17各种情况下独立选自延长剂L,C1-C18烷基,C1-C18烷氧基,或者卤素;以及
(iii)q是整数,其选自0,1,2,3,和4;以及
(h)表示为:
-[S1]c-[Q1-[S2]d]d’-[Q2-[S3]e]e’-[Q3-[S4]f]f’-S5-P的延长剂L,其中:
(i)各Q1,Q2和Q3在各情况下独立地选自:从未被取代的或取代的芳基、未被取代的或取代的脂环族基、未被取代的或取代的杂环基团以及它们的混合基团中选择的二价基团,其中取代基选自:由P表示的基团,液晶基团,卤素,多(C1-C18烷氧基),C1-C18烷氧基羰基,C1-C18烷基羰基,C1-C18烷氧基羰基氧基,芳氧基羰基氧基,全氟(C1-C18)烷氧基,全氟(C1-C18)烷氧基羰基,全氟(C1-C18)烷基羰基,全氟(C1-C18)烷基氨基,二(全氟(C1-C18)烷基)氨基,全氟(C1-C18)烷基硫基,C1-C18烷基硫基,C1-C18酰基,C3-C10环烷基,C3-C10环烷氧基,被氰基、卤素或C1-C18烷氧基单取代或被卤素多取代的直链或支化C1-C18烷基,和含下列通式中的一种的基团:-M(T)(t-1)和-M(OT)(t-1),其中M选自铝,锑,钽,钛,锆和硅,T选自有机官能化基团,有机官能化烃基,脂族烃基和芳族烃基,以及t是M的价态;
(ii)c,d,e和f各自独立地选自0-20中的整数,包括端值;各S1,S2,S3,S4和S5在各情况下独立地选自下列这些的间隔单元:
(1)-(CH2)g-,-(CF2)h-,-Si(CH2)g-,-(Si[(CH3)2]O)h-,
其中g在各情况下独立地选自1到20;h是选自1到16的整数,包括端值;
(2)-N(Z)-,-C(Z)=C(Z)-,-C(Z)=N-,-C(Z′)-C(Z′)-,或者单键,其中Z在各情况下独立地选自氢,C1-C18烷基,C3-C10环烷基和芳基,和Z′在各情况下独立地选自C1-C18烷基,C3-C10环烷基和芳基;和
(3)-O-,-C(O)-,-C≡C-,-N=N-,-S-,-S(O)-,-S(O)(O)-,-(O)S(O)-,-(O)S(O)O-,-O(O)S(O)O-,或直链或支化C1-C24亚烷基残基,所述C1-C24亚烷基残基是未被取代的,被氰基或卤素单取代,或被卤素多取代;条件是,当两个包括杂原子的间隔单元联接在一起时,该间隔单元在联接时要求杂原子不直接联接于彼此之上以及当S1和S5分别地联接到PC和P上时,它们在联接时要求两个杂原子不直接联接于彼此之上;
(iii)P选自:羟基、氨基、C2-C18烯基、C2-C18炔基、叠氮基、甲硅烷基、甲硅烷氧基、甲硅烷基氢化物、(四氢-2H-吡喃-2-基)氧基、硫醇基、异氰酸根合、硫代异氰酸根合、丙烯酰氧基、甲基丙烯酰氧基、2-(丙烯酰氧基)乙基氨基甲酰基、2-(甲基丙烯酰氧基)乙基氨基甲酰基、氮丙啶基、烯丙氧基羰氧基、环氧基、羧酸、羧酸酯、丙烯酰氨基、甲基丙烯酰氨基、氨羰基、C1-C18烷基氨羰基、氨羰基(C1-C18)亚烷基、C1-C18烷氧基羰基氧基、卤代羰基、氢、芳基、羟基(C1-C18)烷基、C1-C18烷基、C1-C18烷氧基、氨基(C1-C18)亚烷基、C1-C18烷基氨基、二-(C1-C18)烷基氨基、C1-C18烷基(C1-C18)烷氧基、C1-C18烷氧基(C1-C18)烷氧基、硝基、聚(C1-C18)烷基醚、(C1-C18)烷基(C1-C18)烷氧基(C1-C18)亚烷基、聚氧化乙烯、聚氧化丙烯、乙炔基、丙烯酰基、丙烯酰氧基(C1-C18)亚烷基、甲基丙烯酰基、甲基丙烯酰氧基(C1-C18)亚烷基、2-氯代丙烯酰基、2-苯基丙烯酰基、丙烯酰基亚苯基、2-氯代丙烯酰氨基、2-苯基丙烯酰氨基羰基、oxetanyl、缩水甘油基、氰基、异氰酸根合(C1-C18)烷基、衣康酸酯、乙烯基醚、乙烯基酯、苯乙烯衍生物、主链和侧链液晶聚合物、硅氧烷衍生物、乙撑亚胺衍生物、马来酸衍生物、富马酸衍生物、未取代肉桂酸衍生物、用甲基、甲氧基、氰基以及卤素至少之一取代的肉桂酸衍生物、或者取代或者未被取代的手性的或者非手性的单价的或者二价基团,其选自类固醇基团、萜类化合物基团、生物碱基团及其混合物,其中该取代基独立地选自C1-C18烷基、C1-C18烷氧基、氨基、C3-C10环烷基、C1-C18烷基(C1-C18)烷氧基、氟代(C1-C18)烷基、氰基、氰基(C1-C18)烷基、氰基(C1-C18)烷氧基或其混合物,或者P是一种结构,其具有2-4个反应性基团或者P是未被取代的或者取代的开环易位聚合前体;以及
(iv)d′,e′和f′各自独立地选自0,1,2,3和4,前提条件是d′+e′+f′的总和至少是1;
(C)如果当所述光致变色材料由图解式I表示时:
(a)Q包含-CN,以及图解式I所述光致变色材料在12-位基本上不含取代基,或者Q包含-N3、-COOR′、-CCR′、-C(R′)C(R′)R′、-OCOR′、-OCOOR′、-SR′、以及-OSO2R′″;
(b)基团A表示茚并,噻吩并,苯并噻吩并,呋喃并或苯并呋喃并;以及
(c)B以及B′各自独立地选自:
(i)氢、C1-C18烷基、C2-C18烷叉、C2-C18次烷基、乙烯基、C3-C10环烷基、C1-C18卤代烷基、烯丙基、卤素以及未被取代的或者用C1-C18烷基以及C1-C18烷氧基至少之一单取代的苄基;
(ii)苯基,其是在对位用至少一种取代基单取代的,该取代基选自:C1-C18烷氧基、直链或者支链C1-C20亚烷基、直链或者支链C1-C4聚氧化烯基、环状的C3-C20亚烷基、亚苯基、亚萘基、C1-C18烷基取代的亚苯基、单或者多氨基甲酸酯(C1-C20)亚烷基、单或者多酯(C1-C20)亚烷基、单或者多碳酸酯(C1-C20)亚烷基、聚亚硅烷基、聚亚硅氧烷基及其混合物,其中该至少一种取代基连接至光致变色材料的芳基;
(iii)-CH(CN)2以及-CH(COOX1)2,其中X1选自延长剂L、氢、未被取代的或者用苯基单取代的C1-C18烷基、用C1-C18烷基、C1-C18卤代烷基或者C1-C18烷氧基单取代的苯基(C1-C18)烷基、以及未被取代的芳基、单或者二取代的芳基的至少之一,其中各芳基取代基独立地选自C1-C18烷基以及C1-C18烷氧基;以及延长剂L;
(iv)-CH(X2)(X3),其中:
(1)X2选自延长剂L,氢,C1-C18烷基,未取代、单-或双-取代的芳基至少之一,其中芳基的各取代基独立选自C1-C18烷基以及C1-C18烷氧基;以及
(2)X3选自-COOX1,-COX1,-COX4,和-CH2OX5中的至少一种,其中:
X4选自下列的至少一种:吗啉代,哌啶子基,未被取代的或被C1-C18烷基单-或二-取代的氨基,以及选自苯基氨基和二苯基氨基中的未被取代的、单或二-取代的基团,其中各取代基独立地选自C1-C18烷基或C1-C18烷氧基;和
X5选自延长剂L,氢,-C(O)X2,未被取代的或被(C1-C18)烷氧基或苯基单取代的C1-C18烷基,被(C1-C18)烷氧基单取代的苯基(C1-C18)烷基,以及未被取代的,单-或二-取代的芳基,其中各芳基取代基独立地选自C1-C18烷基和C1-C18烷氧基;
(v)未被取代的,单-,二-,或三-取代的芳基;9-久洛尼定基(julolidinyl);或选自吡啶基、呋喃基、苯并呋喃-2-基、苯并呋喃-3-基、噻吩基、苯并噻吩-2-基、苯并噻吩-3-基、二苯并呋喃基、二苯并噻吩基、咔唑基、苯并吡啶基、二氢吲哚基或芴基的单-或二-取代的杂芳基,其中各个芳基和杂芳基的取代基在各情况下独立地选自:
(1)延长剂L;
(2)-COOX1或者-C(O)X6;
(3)芳基,卤芳基,C3-C10环烷基芳基,以及被C1-C18烷基或C1-C18烷氧基单-或二-取代的芳基;
(4)C1-C18烷基,C3-C10环烷基,C3-C10环烷氧基(C1-C18)烷基,芳基(C1-C18)烷基,芳氧基(C1-C18)烷基,单-或二-(C1-C18)烷基芳基(C1-C18)烷基,单-或二-(C1-C18)烷氧基芳基(C1-C18)烷基,C1-C18卤代烷基,和单(C1-C18)烷氧基(C1-C18)烷基;
(5)C1-C18烷氧基,C3-C10环烷氧基,环烷氧基(C1-C18)烷氧基,芳基(C1-C18)烷氧基,芳氧基(C1-C18)烷氧基,单-或二-(C1-C18)烷基芳基(C1-C18)烷氧基,和单-或二-(C1-C18)烷氧基芳基(C1-C18)烷氧基;
(6)氨羰基,氨羰基(C1-C18)亚烷基,氨基,单-或者二-烷基氨基,二芳基氨基,哌嗪并(piperazino),N-(C1-C18)烷基哌嗪并,N-芳基哌嗪并,吖丙啶并(aziridino),吲哚并(indolino),哌啶并,吗啉代,硫代吗啉代,四氢化喹啉并(tetrahydroquinolino),四氢化异喹啉并(tetrahydroisoquinolino),吡咯烷基,羟基,丙烯酰氧基,甲基丙烯酰氧基以及卤素;
(7)-OX7或者-N(X7)2;
(8)-SX11;
(9)由式i表示的含氮环;
(10)式ii或者iii表示的基团;
(11)未被取代的或者单取代的基团,选自吡唑基、咪唑基、吡唑啉基、咪唑啉基、吡咯烷基、吩噻嗪基、phenoxazinyl、吩嗪基、或者吖啶基,其中各取代基独立地选自延长剂L,C1-C18烷基,C1-C18烷氧基,苯基,羟基,氨基或者卤素;
(12)式iv或者v表示的基团:
其中:
(I)V′独立地选自各式:-O-,-CH-,C1-C6亚烷基,以及C3-C10亚环烷基,
(II)V独立地选自各式:-O-或者-N(X21)-,其中X21是延长剂L,氢,C1-C18烷基,以及C2-C18酰基,条件是如果V是-N(X21)-,V’是-CH2-,
(III)X18和X19各自独立地选自延长剂L,氢和C1-C18烷基,和
(IV)k选自0,1,和2,以及各X20在各情况下独立地选自延长剂L,C1-C18烷基,C1-C18烷氧基,羟基和卤素;
(13)由式vi表示的基团:
其中
(I)X22选自延长剂L,氢和C1-C18烷基,和
(II)X23选自延长剂L以及选自萘基,苯基,呋喃基和噻吩基中的未被取代的或单-或二-取代的基团,其中各取代基在各情况下独立地选自C1-C18烷基,C1-C18烷氧基,和卤素;以及
(14)B和B′一起形成未取代的、单-或二-取代的芴-9-叉或形成饱和的C3-C12螺-单环烃环,例如环丙叉,环丁叉,环戊叉,环己叉,环庚叉,环辛叉,环壬叉,环癸叉,环十一烷叉,环十二烷叉,饱和的C7-C12螺-二环烃环,如二环[2.2.1]庚叉,即降冰片叉,1,7,7-三甲基二环[2.2.1]-庚叉,即冰片叉,二环[3.2.1]辛叉,二环[3.3.1]壬-9-基叉,二环[4.3.2]十一烷,以及饱和的C7-C12螺-三环烃环,例如三环[2.2.1.02,6]庚叉,三环[3.3.1.13,7]癸叉,即金刚烷叉,和三环[5.3.1.12,6]十二烷叉;和延长剂L,其中芴-9-叉上的取代基可以选自C1-C4烷基,C1-C4烷氧基,溴,氟和氯。
(D)如果当所述光致变色材料通过图解式II表示时,Q包含-N3或者-OCOOR′,条件是图解式II所述光致变色材料在5-位置基本上无取代基;以及R,i,B和B′同以上所述;
(E)如果当所述光致变色材料通过图解式III表示时,Q对于各个情况独立地包含-N3或者-OCOOR′;以及R,i,B和B′同上文;
(F)如果当所述光致变色材料通过图解式IVA或者IVB表示时,Q对于各个情况独立地包含-N3;或者-CCR′,条件是该吲哚并基团基本上不含N-取代基;或者-OSO2R″′,条件是所述光致变色材料基本上不含羰基以及各R″在各个情况下独立选自:氢,取代的或者未被取代的烷基,环烷基,芳基烷基,或者一起形成取代的或者未被取代的环烷基;以及R和i同上文;
(G)如果当所述光致变色材料通过图解式V表示时,Q包含-N3,-CN,-CCR′,或者-OSO2R″′;以及R,i,B和B′同上文;以及
(H)如果当所述光致变色材料通过图解式VI表示时,Q包含:-N3,-CN,-CCR′,或者-OSO2R″′;E是-O-或者-N(Q)-;以及D由以下图解式表示:
其中:T是-S-,-O-或者-N(R)-,J是螺-脂环和Q同上文所述。
根据一种特定的、非限制实施方案所述,其中该光致变色的基团包含至少两PCs,该PCs可以经由在各PCs上连接基取代基彼此连接。例如,该PCs可以是可聚合光致变色基团或者光致变色基团其适合于与基质材料(host material)相容(″可相容的光致变色基团″)。可聚合光致变色基团的非限制性实例由其PC可以选择而且用于本申请公开的非限制实施方案是公开在美国专利US6,113,814中,在本文中明确将其引入作为参考本申请。从其中可以选择PC而且与本申请所公开各种非限制实施方案中应用的有关的相容光致变色基团的非限制性实例公开在专利号为US6,555,028的美国专利中,其明确引入本申请作为参考。
其它的适合的光致变色的基团以及补充的光致变色的基团公开在美国专利US6,080,338中的第2栏,第21行至第14栏,第43行;US6,136,968的第2栏,第43行至第20栏,第67行;US 6,296,785的第2栏,第47行至第31栏,第5行;US 6,348,604的第3栏,第26行至第17栏,第15行;US 6,353,102的第1栏,第62行至第11栏,第64行;以及US 6,630,597的第2栏,第16行至第16栏,第23行;上述专利的说明书引入本文作为参考。
另一非限制实施方案提供连接于至少一种光致变色的基团的上述延长剂(L),其中该至少一种延长剂选自一种下列化合物(图解表示):
本申请公开的另一非限制实施方案提供通过以下图解式表示的图解式I光致变色化合物:
另外,根据本申请公开的各种非限制实施方案,通过式I,II,III,IVA,IVB,V和VI表示的光致变色化合物可以包含一种或多种延长剂(L)。正如先前提及的,在L中,c,d,e和f可以各自独立地选自1-20中的整数,包括端值;和d′,e′和f′可以各自独立地选自0,1,2,3和4,前提条件是d′+e′+f′的总和至少是1。根据本申请公开的其它的非限制实施方案,c,d,e和f可以各自独立地选自0-20中的整数,包括端值;和d′,e′和f′可以各自独立地选自0,1,2,3和4,前提条件是d′+e′+f′的总和至少是2。根据本申请公开的其它的非限制实施方案,c,d,e和f可以各自独立地选自0-20中的整数,包括端值;和d′,e′和f′可以各自独立地选自0,1,2,3和4,前提条件是d′+e′+f′的总和至少是3。根据本申请公开的其它的非限制实施方案,c,d,e和f可以各自独立地选自0-20中的整数,包括端值;和d′,e′和f′可以各自独立地选自0,1,2,3和4,前提条件是d′+e′+f′的总和至少是1。
由此,例如,在式I,II,III,IVA,IVB,V和VI中,″i″可以至少为1以及R基团至少之一可以是延长剂L。另外或者可替换的是,该光致变色化合物可以包含至少一个R基团,至少一个B基团,或者至少一个延长剂L取代的B′基团。例如,尽管未限制本申请,但是在一种非限制实施方案中,该光致变色化合物可以包含B基团,其包含用延长剂L单取代的苯基.
而且,尽管未限制本申请,但是根据本申请公开的各种非限制实施方案,该延长剂(L)可以在任何可用的位置连接于光致变色基团(例如,式I,II,III或V的吡喃基团)以致L在活化态中延伸或者延长该光致变色基团从而使延长的光致变色基团(即,该光致变色化合物)的吸收比同未延伸的光致变色基团相比得以提高。由此,举例来说而非限制,根据其中该光致变色化合物表示为式I,II,III或V的各种非限制实施方案所说,L可以直接键连至该吡喃基团,例如,其中i至少是1以及R是L,或者可以间接地键连至该吡喃基团,例如,作为在R基团,B,或者B′基团上的取代基以致L在活化态中延长该吡喃基团从而使光致变色化合物的吸收比同未延伸的吡喃基团相比得以提高。
此外,根据本申请所公开各种非限制实施方案以及一般通过式I,II,III,V和VI表示的光致变色化合物在活化态中可以具有至少1.5的平均吸收比,根据CELL法测定。根据其它的非限制性实施方案,该光致变色化合物在活化态中具有的平均吸收比为4-20,3-30,或2.5-50,根据CELL法测定。根据其它的非限制性实施方案,该光致变色化合物可以在活
光致变色化合物专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0