IPC分类号 : C12N1/14,C12P7/00,A61K31/11,A61P39/06,C12R1/645
专利摘要
本发明提供了一株球毛壳菌及其次生代谢产物黄柄曲菌素(flavipin)的制备和应用。所述的菌株是自银杏叶片分离获得的内生真菌,经鉴定为球毛壳菌(Chaetomiumglobosum),编号CDW7,该菌株已保藏在中国微生物菌种保藏管理委员会普通微生物中心,登记编号为CGMCCNo.6658。本发明同时涉及CDW7代谢产物黄柄曲菌素的制备和用途。具体制备方法为将菌株CDW7发酵液有机溶剂萃取物经凝胶柱层析和重结晶后获得。黄柄曲菌素(flavipin)具有较强的抗氧化活性,可作为抗氧化剂进行应用。CGMCCNo.66582012.10.15
权利要求
1.一株产黄柄曲菌素(flavipin)的银杏内生真菌球毛壳菌(Chaetomium globosum)CDW7,已保藏于中国微生物菌种保藏管理委员会普通微生物中心,登记编号为CGMCC No.6658。
2.一种制备黄柄曲菌素(flavipin)的方法,其特征在于该化合物采用如下步骤得到:
(1)将保存的球毛壳菌CDW7接种到PDA平板上,25℃培养5天后,取菌丝块于PDB培养基中,25℃,150rpm条件下培养14天。
(2)将步骤(1)所得发酵液过滤,滤液用二氯甲烷萃取,减压浓缩获得发酵物粗浸膏F1。
(3)将步骤(2)中的发酵物粗浸膏F1进行Sepahdex LH-20柱层析,以氯仿/甲醇(体积比1/1)洗脱,经TLC检测,合并含有黄柄曲菌素(flavipin)的组分,减压浓缩得黄色浸膏F2。
(4)将步骤(3)中黄色浸膏F2在丙酮/石油醚(体积比10/1)中重结晶,即得化合物黄柄曲菌素(flavipin)。
3.一种权利要求2所述的黄柄曲菌素(flavipin)在制备抗氧化剂中的应用。
说明书
技术领域
本发明涉及球毛壳真菌及其代谢产物黄柄曲菌素的制备和应用。
背景技术
越来越多的自由基生物学和自由基医学研究结果表明心血管疾病、肿瘤、老年性痴呆、衰老,以及糖尿病、艾滋病等疾病的发生和发展都与活性氧及自由基密切相关,寻找和研制新型、高效、安全的天然抗氧化剂,是预防和治疗与活性氧和自由基密切相关的重大疾病研究的重要课题之一。
植物内生菌是指那些在其生活史的一定阶段或全部阶段生活于健康植物的各种组织和器官内部的真菌或细菌,被感染的宿主植物(至少是暂时)不表现出外在病症,可通过组织学方法从严格表面消毒的植物组织中分离或从植物组织内直接扩增出微生物DNA的方法来证明其内生。内生真菌可产生丰富多样的次生代谢产物,被认为是活性物质的潜在资源,从植物内生真菌中筛选抗氧化的活性菌株及活性代谢产物已引起广泛的关注。毛壳属真菌次生代谢产物的丰富化学多样性,迄今为止,已有120多种次生代谢物从该属真菌发酵物中分离得到,包括生物碱,蒽醌,萜,甾体等多种结构类型,其中有许多化合物都具有显著的生物活性,如抗肿瘤、抗炎、细胞毒性、酶抑制活性、抗菌活性等。本文中涉及的毛壳属真菌Chaetomium globosum CDW7是从健康银杏叶片分离得到的植物内生菌,其次生代谢产物黄柄曲菌素(flavipin,1,2-benzenedicarboxaldehyde-3,4,5-trihydroxy-6-methyl)最早由Raistrick分离自黄柄曲霉(Aspergillus flavipes)和士曲霉(Aspergillus terreus),具有一定的抗菌及杀线虫活性,而其抗氧化活性至今未见报道。
发明内容
本发明的一个目的在于提供一株高产抗氧化活性物质黄柄曲菌素(flavipin)的菌株。本发明提供的高产黄柄曲菌素(flavipin)的菌株CDW7是从经表面消毒的健康银杏叶片中分离、纯化获得的内生真菌。该菌株在PDA平面培养基上,菌落初期为白色,渐变至暗青色,背面褐色,边缘不整齐。子囊壳散生或群生,卵形或近球形,大小(418-610)μm×(222-277)μm;子囊壳壁由暗褐色交错丝状组织构成,顶毛无隔膜,褐色,曲折状或螺旋状卷曲,表面有细刺,基部粗径为3.1μm;子囊孢子褐色,亚球形或柠檬形,大小(7.5-10.2)μm×(6.5-7.5)μm,有一顶生芽孔。上述形态特征符合毛壳菌属(Chaetomium sp.)真菌形态特征(见附图1、附图2、附图3、附图4)。同时测定其ITS序列,与HQ914911Chaetomium globosu序列相似度为100%(见附图5),鉴定为球毛壳菌(Chaetomium globosum,Genbank登录号为JN588554),菌株编号CDW7。该菌株于2012年10月15日保存于中国普通微生物菌种保藏管理中心(简称CGMCC),地址为北京市朝阳区北辰西路1号院3号,保藏号为CGMCC No.6658。
本发明的另外一个目的为提供一种黄柄曲菌素(flavipin)的制备方法和及其在抗氧化剂中的应用。
本发明提供的制备方法,包括下述步骤:
(1)将保存的球毛壳菌(Chaetomium globosum)CDW7接种到PDA平板上,在25℃培养5天后,取菌丝块放入已灭菌装有PDB培养基的三角瓶中,于25℃,150rpm条件下培养14天。
(2)将步骤(1)所得发酵液过滤,滤液用二氯甲烷萃取,真空浓缩获得发酵物粗浸膏F1。
(3)将步骤(2)中的发酵物粗浸膏F1进行Sepahdex LH-20柱层析,以氯仿/甲醇(体积比1/1)洗脱,洗脱下的每个组分经TLC检测,合并含有黄柄曲菌素(flavipin)的组分,减压浓缩得黄色浸膏F2。
所述的TLC展开剂为氯仿/甲醇(体积比10/1),黄柄曲菌素(flavipin)的Rf值为0.55
(4)将步骤(3)中黄色浸膏F2在丙酮/石油醚(体积比10/1)中重结晶,即得化合物黄柄曲菌素(flavipin)。
本发明的实验证明,具有高产黄柄曲菌素(flavipin)的能力,黄柄曲菌素(flavipin)具有很强的抗氧化活性,可作为抗氧化剂进行应用。
附图说明
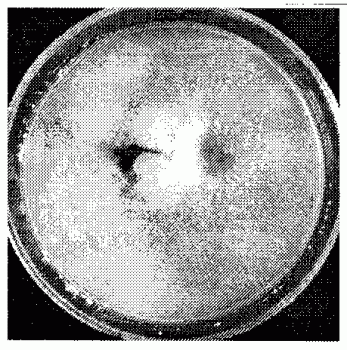
图1为球毛壳菌(Chaetomium globosum)CDW7于PDA培养10天菌落形态。
图2为球毛壳菌(Chaetomium globosum)CDW7于PDA培养25天菌落形态。
图3为球毛壳菌(Chaetomium globosum)CDW7子囊壳。
图4为球毛壳菌(Chaetomium globosum)CDW7菌丝和子囊孢子。
图5为球毛壳菌(Chaetomium globosum)CDW7同源性系统发育树。
具体实施方式
实施例一.内生菌株CDW7的分离纯化:
采集新鲜健康的银杏叶片,洗净后浸泡在75%的酒精中30s,无菌水冲洗3次,再浸入3-5%NaClO溶液3-5min,用无菌水冲洗3-5次。在无菌条件下,将经表面消毒的银杏叶片剪切成0.5×0.5cm的小块,分别置于PDA培养基于25℃恒温培养,待菌体长出后,挑取菌落边缘菌丝纯化培养至菌落形态一致,保存于PDA斜面,得到银杏内生菌。其中一株菌株编号为CDW7,现保存于中国普通微生物菌种保藏管理中心(简称CGMCC),保藏日期为2012年10月15日,保藏号为CGMCCNo.6658。
实施例二.内生菌株CDW7的鉴定:
内生真菌CDW7其在PDA平面培养基上,菌落初期为白色(见附图1),渐变至暗青色(见附图2),背面褐色,边缘不整齐。子囊壳散生或群生,卵形或近球形,大小(418-610)μm×(222-277)μm(见附图3);子囊壳壁由暗褐色交错丝状组织构成,顶毛无隔膜,褐色,曲折状或螺旋状卷曲,表面有细刺,基部粗径为3.1μm;子囊孢子褐色,亚球形或柠檬形,大小(7.5-10.2)μm×(6.5-7.5)μm,有一顶生芽孔(见附图4)。上述CDW7的形态特征符合毛壳菌属(Chaetomium sp.)真菌形态特征。
挑取平板活化的CDW7菌株的菌丝块进入PDB培养基中,25℃培养5天后,采用常规分子生物学方法提取总DNA。运用PCR技术,采用真菌通用正向引物ITS1(5’-TCCGTAGGTGAACCTGCGG-3’)和反向引物ITS4(5’-TCCTCCGCTTATTGATATGC-3’)扩增菌株18S-28S rDNA的ITS区间。经电泳提纯及凝胶回收后,采用ABI PRISM 3730测序仪分别进行正相(5’→3’)和反相(3’→5’)测序。把所得的ITS rDNA序列利用Blast工具进行序列对比,发现该序列与HQ914911Chaetomium globosu的序列相似度为100%,并提交到Genbank数据库(www.ncbi.nlm.nih.gov/genbank/),获得序列号为JN588554(见附图5)。
综合形态学观察和分子生物学实验结果,菌株CDW7鉴定为球毛壳菌(Chaetomium globosum)。
实施例三.化合物黄柄曲菌素(flavipin)的制备:
(1)CDW7的发酵培养:取4℃保存的球毛壳菌CDW7菌种接种到PDA平板上,在25℃恒温培养箱中培养5天,在平板上取直径为0.5cm的菌饼12个块放入已灭菌装有100mL PDB培养基的250mL三角瓶中,在25℃、150rpm条件下培养14天。
(2)发酵物粗浸膏的获得:取上述步骤(1)获得的发酵液,用纱布将菌体和发酵液分离,得总发酵滤液2L,将发酵滤液用二氯甲烷溶剂萃取3-5次,合并萃取液进行减压浓缩,获得发酵物粗浸膏F1(2g)。
(3)化合物的分离纯化:将上述步骤(2)获得的发酵物粗浸膏进行sephadex LH-20层析,以氯仿/甲醇(体积比1/1)洗脱,洗脱下的每个组分经TLC检测,合并含有黄柄曲菌素(flavipin)的组分,减压浓缩得黄色浸膏F2。其中,TLC展开剂为氯仿/甲醇(体积比10/1),黄柄曲菌素(flavipin)的Rf值为0.55。将黄色浸膏F2在丙酮/石油醚(体积比10/1)中重结晶,即得化合物黄柄曲菌素(flavipin,50mg)。
实施例四.化合物黄柄曲菌素(flavipin)的结构鉴定:
用实施例三所获得化合物为黄色晶体,m.p.223-224℃,根据质谱、核磁共振谱鉴定为黄柄曲菌素(flavipin,1,2-benzenedicarboxaldehyde-3,4,5-trihydroxy-6-methyl),光谱数据如下:
ESI-MS:m/z 197.0560[M+H+]。
1H-NMR(400MHz,Acetone-d6)δ(ppm):2.50(3H,s),10.38(1H,s),10.59(1H,s)。
13C-NMR(100MHz,Acetone-d6)δ(ppm):10.25(C-7),113.09(C-2),124.58(C-6),129.04(C-1),136.46(C-4),150.28(C-3),151.32(C-5),192.91(C-9),197.50(C-8)。
实施例五.抗氧化实验:分别采用DPPH、FRAP、ABTS和ORAC法测定黄柄曲菌素(flavipin)抗氧化活性,以BHT和vitamin C作为阳性对照。试验方法如下
DPPH自由基清除法测定抗氧化活性:于96孔板中,分别加入100μL梯度稀释样品溶液和100μL2×10-4mol/L的DPPH溶液(A测),100μL样品溶液中和100μL无水乙醇(A样),100μL DPPH溶液和100μL无水乙醇(A空白),25℃反应30min后,使用酶标仪测定517nm处吸光值,重复三次,按照公式SC%=[1-(A测-A样)/A空白]×100%计算清除率。结果以IC50表示,即当达到50%的DPPH自由基清除率时,待测样品液(抗氧化剂)的浓度。
FRAP法测定抗氧化活性:于96孔板中,分别加入20μL梯度稀释样品溶液和180μLFRAP工作液(300mmol/L pH 3.6醋酸盐缓冲液/10mmol/L TPTZ/20mmol/L FeCl3,体积比10/1/1,现配现用),37℃反应4min后用酶标仪测定593nm处吸光值,重复三次。以FeSO4·7H2O标准曲线作为参考(0.1-1.0mmol/L,n=6,标准曲线为Y=1.2273X+0.0460,R2=0.9994),结果以C0.5FRAP表示,即具有0.5mmol/L FeSO4·7H2O抗氧化能力的样品浓度。
ABTS法测定抗氧化活性:ABTS·+由5mL 7mmol/L ABTS溶液和88μL 140mmol/L K2S2O8水溶液避光反应12小时后生成,用乙醇稀释(732nm处吸光值为0.70±0.02)。取20μL梯度稀释样品溶液加到180μLABTS·+溶液中避光反应10min后测定732nm吸光值,最终结果以IC50表示,即当达到50%的ABTS·+自由基清除率时,待测样品液(抗氧化剂)的浓度。
ORAC法测定抗氧化活性:配置160mmol/L AAPH磷酸缓冲溶液(pH=6.9)和4×10-3mmol/L荧光素纳磷酸缓冲溶液(pH=6.9),避光低温保存,使用前用磷酸缓冲溶液稀释10000倍。于96孔黑色微孔板中加入25μL梯度稀释样品液和150μL的荧光素钠液,再加入25μL AAPH诱发荧光淬灭,使用SpectraMax M5荧光酶标仪(设置参数为:激发波长485nm,发射波长528nm,37℃;循环数:35;循环周期:120s)进行测定。实验结果以抗氧化能力指数(ORAC)表示。ORAC指数是指在抗氧化剂存在下,荧光衰退曲线上受保护积分面积(需统一换算1μmol/L Trolox的保护面积)的大小,1个ORAC单位定义为:终浓度为1μmol/L的Trolox在荧光衰退曲线上对应的保护积分面积。
化合物黄柄曲菌素(flavipin)抗氧化测试结果如表1所示:
表1化合物黄柄曲菌素(flavipin)抗氧化活性
字母上标表示5%水平显著性差异
上述实验证明,化合物黄柄曲菌素(flavipin)具有与vitamin C相当的抗氧化活性,其作为新型抗氧化剂具有巨大的潜力。
一株球毛壳菌及其代谢产物黄柄曲菌素的制备和应用专利购买费用说明
![]()
Q:办理专利转让的流程及所需资料
A:专利权人变更需要办理著录项目变更手续,有代理机构的,变更手续应当由代理机构办理。
1:专利变更应当使用专利局统一制作的“著录项目变更申报书”提出。
2:按规定缴纳著录项目变更手续费。
3:同时提交相关证明文件原件。
4:专利权转移的,变更后的专利权人委托新专利代理机构的,应当提交变更后的全体专利申请人签字或者盖章的委托书。
Q:专利著录项目变更费用如何缴交
A:(1)直接到国家知识产权局受理大厅收费窗口缴纳,(2)通过代办处缴纳,(3)通过邮局或者银行汇款,更多缴纳方式
Q:专利转让变更,多久能出结果
A:著录项目变更请求书递交后,一般1-2个月左右就会收到通知,国家知识产权局会下达《转让手续合格通知书》。
动态评分
0.0